Фармацевтическая отрасль давно живёт в условиях обязательной маркировки лекарств, но правила и требования продолжают меняться. Впервые специалисты столкнулись с этим понятием в 2015 году, а с 2017 года, после принятия закона 425-ФЗ, процесс стал обязательным. Теперь система Мониторинга движения лекарственных препаратов (МДЛП) отслеживает каждую упаковку на всех этапах — от производителя до конечного покупателя.
А как обстоит ситуация в 2025 году? В статье мы расскажем про действующие правила маркировки товаров аптечного ассортимента, последние новости и требования к маркировке лекарственных средств и других товаров аптечного ассортимента. Помимо этого мы рассмотрели особенности участников системы мониторинга и ответили на популярные вопросы.
Содержание
Документы
Маркировка — это нанесение производителем или импортёром на продукт, вторичную или транспортную упаковку специальной марки, которая является идентификатором, подтверждающим подлинность товара.
Функции маркировки на фармацевтическом рынке
Ещё несколько лет назад для защиты от подделок производители использовали сложные виды упаковки, голограммы, специальные шрифты и водяные знаки. Но даже такие методы не давали полной гарантии защиты от фальсификатов. Маркировка лекарств вывела контроль на новый уровень: теперь у каждой упаковки есть уникальный код, который невозможно подделать.
Система МДЛП позволяет отслеживать весь путь препарата — от производства до продажи. С её помощью можно исключить из оборота лекарства, данные о которых отсутствуют или не соответствуют требованиям, и проверить подлинность упаковки с помощью сканирования кода Data Matrix. Для покупателей маркировка даёт уверенность в качестве препаратов, а для фармацевтов она является удобным инструментом проверки подлинности товара прямо в аптеке.
Основные функции маркировки заключаются в защите рынка от попадания некачественных лекарственных препаратов или товаров аптечного ассортимента и в предоставлении возможности каждому участнику оборота проверить подлинность товара, его производителя и срок изготовления.
В ст. 4 Федерального закона от 12.04.2010 № 61 «Об обращении лекарственных средств» определено три группы некачественных лекарственных препаратов:
- недоброкачественные — лекарство, которое не соответствует требованиям фармакопейной статьи, нормативной документации или нормативного документа;
- контрафактные — лекарство, которое находится в обороте с нарушением гражданского законодательства;
- фальсифицированные — лекарство, которое сопровождается ложной информацией о производителе или составе.
Фальсифицированные и контрафактные препараты чаще всего производятся нелегально, а значит, их качество и безопасность никто не проверяет. Именно поэтому их наличие на рынке несёт серьёзную угрозу здоровью покупателей.
Статья 46. Маркировка лекарственных средств
12. На вторичную (потребительскую) упаковку лекарственного препарата наносится штриховой код.
Федеральный закон № 61-ФЗ «Об обращении лекарственных средств»
Именно с целью повышения безопасности лекарственных препаратов, на фармацевтическом рынке России была внедрена система маркировки при помощи специальных кодов.
Код маркировки. Что это и как выглядит?
В ходе маркировки на упаковку товара наносят уникальный двухмерный Data Matrix код. Код этого формата содержит защищённую криптографическим образом информацию и полностью соответствует международным стандартам и критериям защищённости.
DataMatrix — это двумерный матричный штрих-код в виде чёрно-белых элементов или элементов различных степеней яркости, обычно представленный в форме квадрата. Матричный штрих-код применяется для кодирования текста и данных других типов.
Код наносит производитель товара на вторичной упаковке, а при её отсутствии — на первичной.
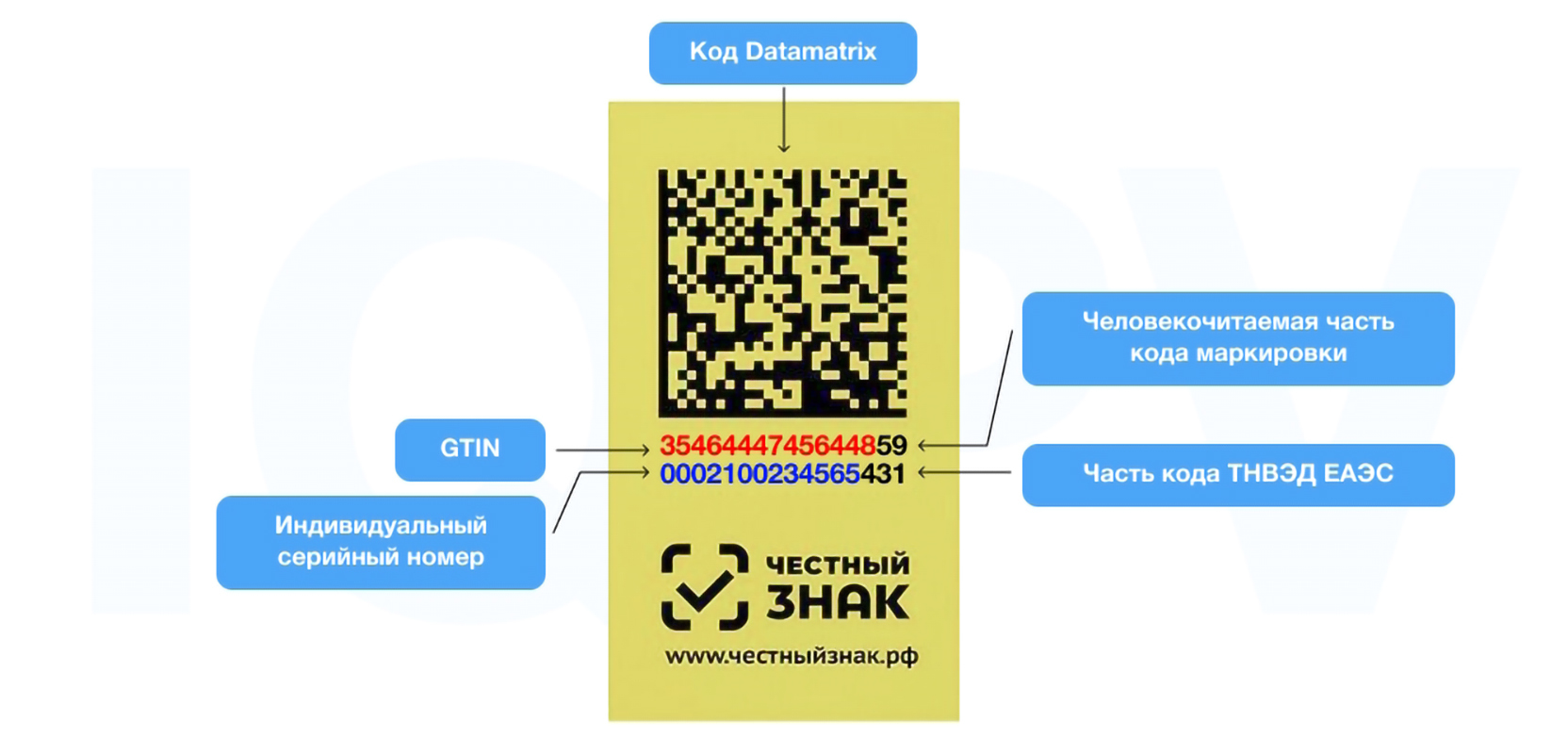
Внешне Data Matrix код поход на двухмерный матричный идентификатор, состоящий из четырех частей. Нанесённый на упаковку лекарства код должен иметь размерность 36 на 36 модулей. Он включает:
- GTIN (Global Trade Item Number — международный код маркировки товарной позиции, который присваивается по стандарту GS1) — 14 символов;
- индивидуальный серийный номер препарата — 13 символов;
- ключ поставки — 4 цифры;
- проверочный код из цифр или сочетания цифр и букв — 44 символа.
Общая длина идентификационного знака составляет 83 символа. Рекомендованный размер кода Data Matrix ― 16×16 мм, однако допустимы и меньшие размеры.
На большую транспортную тару, такую как паллеты или коробки, наносятся коды формата GS1 128, в которых содержится информация обо всех упаковках.
Коды Data Matrix применяются при операциях по приёмке, передаче, перемещении и выводу лекарственных средств из оборота. Чтобы узнать статус товара, нужно отсканировать код при помощи сканера или мобильного приложения системного мониторинга «Честный знак». Считывание кода производится на каждом этапе движения товара.
Товары аптечного ассортимента, подлежащие маркировке
Маркировка товаров аптечного ассортимента в России становится всё более масштабной и охватывает всё новые группы продукции. Если изначально она касалась только лекарственных препаратов, то со временем в этот список вошли биологически активные добавки (БАДы), детское питание, антисептики, медицинские изделия, вода и многие другие товары, реализуемые в аптеках.
Лекарственные препараты — первая и самая очевидная категория товаров, требующая строгого контроля. В России с 1 июля 2020 года действует обязательная маркировка лекарств в системе «Честный знак». Такая мера направлена на борьбу с фальсификатом и обеспечение безопасности пациентов.
Поправки в ст. 57 Федерального закона № 61-ФЗ «Об обращении лекарственных средств» от 12 апреля 2010 года напрямую запрещают продавать лекарства без маркировки или с неправильной маркировкой. Ограничения не распространяются на препараты, предназначенные для лечения пациентов с тяжёлыми заболеваниями, такими как гемофилия, муковисцидоз, болезнь Гоше, злокачественные заболевания крови, рассеянный склероз и др. Также под запрет не попадают лекарства для людей после трансплантации органов и тканей (если они были произведены до 31 декабря 2019 года).
|
Категория товара |
Примеры |
|---|---|
|
Лекарственные препараты |
Таблетки, капсулы, сиропы, инъекционные растворы. |
|
Медицинские изделия |
Обеззараживатели воздуха, ортопедическая обувь, стельки и вкладыши к ней, слуховые аппараты, санитарно-гигиенические изделия для людей с недержанием. |
|
Биологически активные добавки (БАД) |
Витаминные и минеральные комплексы, растительные экстракты и так далее. |
|
Антисептики и дезинфицирующие средства |
Парфюмерно-косметическая продукция для гигиены рук с антимикробным действием, кожные антисептики (код ОКПД2 20.20.14.000, код ТН ВЭД ЕАЭС 3808 94 800 0). С 1 марта добавятся кожные антисептики (коды ТН ВЭД ЕАЭС 3808 94 100 0, 3808 94 300 0). |
|
Фармацевтическое сырьё |
Растительное сырьё для изготовления лекарственных средств, антибиотики, глюкоза, пропиленгликоль. |
|
Упакованная вода |
Вода в бутылках, которую можно предложить покупателю. |
|
Медицинские перчатки |
С 1 марта 2025 года. |
Обратите внимание, что перечень товаров, подлежащих обязательной маркировке, может обновляться. Рекомендуем регулярно проверять актуальную информацию на официальном сайте системы маркировки «Честный ЗНАК».
Маркировка лекарств остаётся самым строгим направлением контроля, поэтому аптеки должны чётко следить за правильностью учёта данных в системе «Честный Знак».
Кто участвует в системе маркировки?
В обороте маркированных фармацевтических товаров участвуют:
- производители;
- оптовые компании;
- розничные точки — аптеки;
- медицинские организации.
Каждая категория имеет свои особенности учёта.
Как работает система маркировки?
Идентификатор к товару привязывают производители или импортёры, после чего он поступает к оптовикам и в розничные точки. Каждый участников оборота должен зафиксировать операции, которые совершаются над маркированным товаром.
Как правило, фиксируется две основные операции: приёмка и отпуск потребителю. В случае аптеки к таким операциям относятся приёмка товара от оптового поставщика и отпуск физическому лицу. Каждый участник оборота для регистрации операций использует специальные квалифицированные электронные подписи (КЭП).
Таким образом формируется логистическая цепочка, которая позволяет проследить путь промаркированного товара от производителя к конечному потребителю. Несанкционированному участнику, например изготовителю фальсифицированных лекарственных средств, очень сложно «вклиниться» в эту цепочку, так как незаметно получить и использовать КЭП законного участника оборота практически невозможно.
Прочитать QR-код на упаковке и отследить логистическую цепочку может каждый участник, включая конечного покупателя.

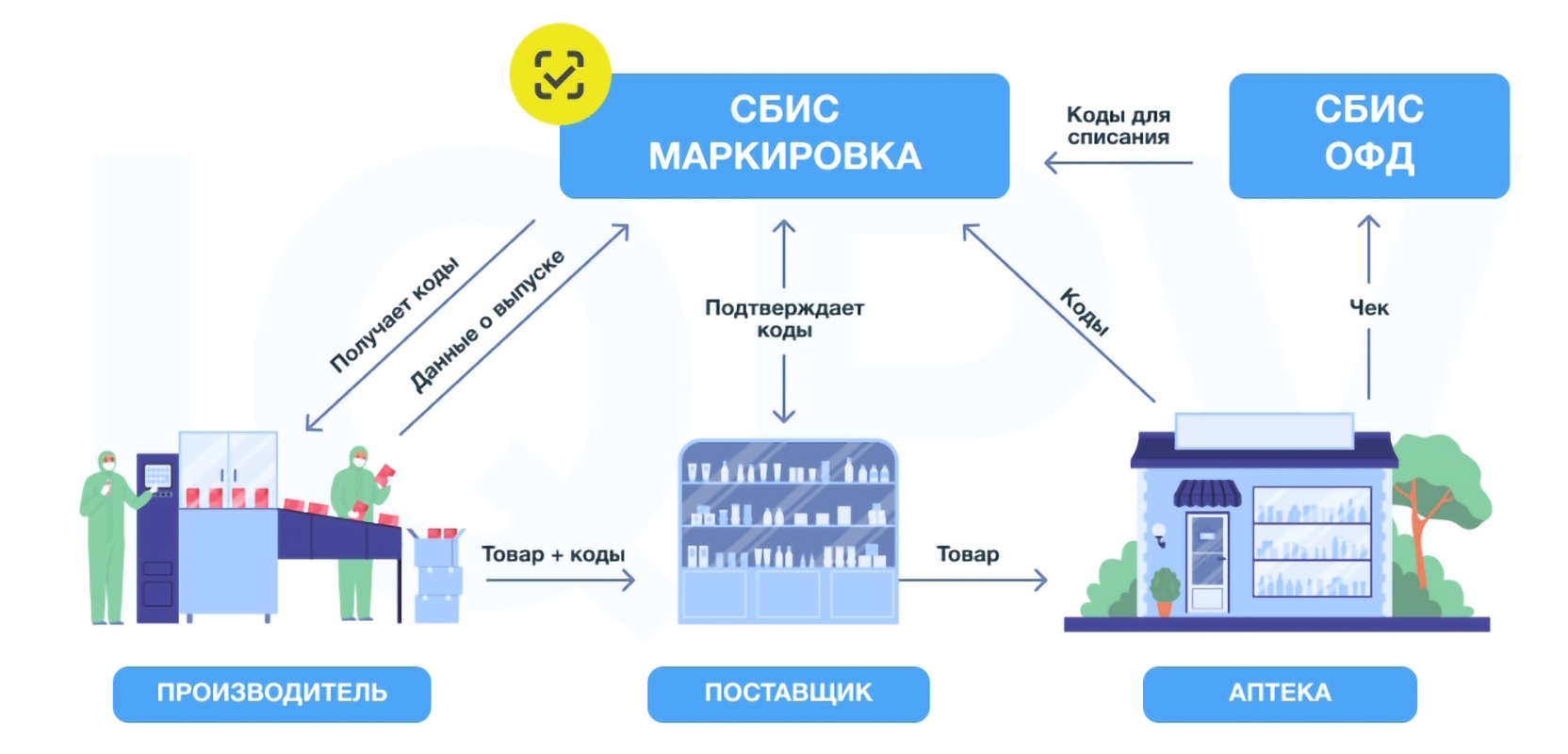
Можно выделить общую схему взаимодействия между участниками оборота:
- Производитель получает коды в системе маркировки и размещает их на упаковках лекарственных препаратов.
- Во время отгрузки вместе с товаром производитель передаёт дистрибьютору список кодов.
- Дистрибьютор проводит приёмку товара и подтверждает получение кодов.
- Дистрибьютор выполняет расфасовку товара и направляет его в аптеку.
- Аптека проводит приёмку, во время которой происходит сканирование кодов с упаковок лекарств.
- Отсканированные коды направляются поставщику в систему МДЛП (Мониторинг Движения Лекарственных Препаратов).
- При отпуске и продаже фармацевт или провизор сканирует код маркировки на упаковке, после чего оператор фискальных данных отправляет его в систему маркировки.
- Код выбывает из оборота.
Таким образом отслеживается весь путь перемещения лекарственных препаратов, начиная с момента производства и до их получения покупателями. Контролирующие органы в любой момент времени смогут узнать, где находится фармацевтический товар и сколько времени осталось до окончания срока его годности.
Отгрузка лекарственных средств может проходить по прямому или обратному акцепту:
- прямой порядок акцептования («прямой акцепт»). Сведения об отгрузке товара регистрируются отправителем. Получатель подтверждает зарегистрированные в системе сведения;
- обратный порядок акцептования («обратный акцепт»). Сведения об отгрузке товара регистрируются получателем. Отправитель подтверждает зарегистрированные в системе сведения.
«Прямой акцепт» более точен, так как проверка штрих-кодов производится как со стороны получателя, так и со стороны отправителя. Это уменьшает вероятность возникновения пересортицы. Но не все дистрибьюторы готовы к такой форме работы — для этого требуется дополнительные оборудование и персонал.
Поэтому «Обратный акцепт» остаётся самым распространённым способом взаимодействия дистрибьютора с аптечными сетями. Аптека, получив поставку, должна просканировать все упаковки товара в рамках одной накладной, сформировать документ установленного вида и отправить его в систему мониторинга движения лекарственных средств. Эта информация сверяется с данными, которые вносит дистрибьютор. Если данные совпадают — считается, что поставка состоялась. Аптека получает сообщение, что поставка принята.
На июнь 2024 года благодаря системе маркировки возможностью по приостановке оборота серий некачественных лекарств воспользовались порядка 400 раз, из которых только 10 случаев были отменены.
Программа маркировки лекарственных препаратов даёт возможность быстро принять партию лекарственных средств и других товаров аптечного ассортимента любого объёма. Специализированное программное обеспечение позволяет провести приём и отказ от приёма, возврат и выбытие товаров, а также узнать статус маркировочного кода препарата.

Розничная продажа лекарств в аптеках
Система мониторинга маркированных товаров имеет несколько видов вывода лекарственных препаратов из оборота:
- розничная продажа — аптека отпустила товар покупателю за полную стоимость;
- льготный отпуск — аптека отпустила товар покупателю за частичную стоимость;
- вывод из оборота для оказания медицинской помощи — вывод лекарства из-за использования медицинской организацией для предоставления медицинской помощи;
- вывод из оборота по иным причинам.
К иным причинам относится уничтожение препарата и списание без передачи на уничтожение, недостача, производственный брак, частичное списание и так далее.
Для «вывода» лекарства из оборота аптеке требуется контрольно-кассовая техника, актуальное кассовое программное обеспечение и сканер для считывания 2D-кодов.
Особых различий в реализации аптекой лекарственных препаратов и других товаров нет. Фармацевт или провизор при отпуске товара сканирует код маркировки, который вместе с другой информацией автоматически поступает в систему мониторинга. Передача сведений происходит в несколько этапов:
- при расчёте с покупателем формируются фискальный документ и кассовый чек;
- фискальный документ шифруется и передаётся ОФД (Оператору фискальных данных), а затем поступает в ФНС (Федеральную налоговую службу);
- ФНС подтверждает операцию и передаёт сведения в систему мониторинга.

Чтобы избежать ошибок при реализации товара, рекомендуется придерживаться следующего алгоритма действий при отпуске маркированных товаров:
- Получение запроса от покупателя и предоставление фармацевтической консультации.
- Подобрать подходящие покупателю лекарственные препараты и получить его согласие на их покупку.
- Последовательно считать при помощи сканера коды маркировки DataMatrix с каждой упаковки лекарственных препаратов. При повторном сканировании одной и той же упаковки регистратор выбытия не добавит её в список для вывода из оборота, а сообщит об ошибочном сканировании.
- Проверить корректность считывания кодов маркировки.
- Получить оплату за товары аптечного ассортимента и пробить кассовый чек.
- Передать покупателю товар, сдачу и кассовый чек.
Вопросы и ответы
Что делать, если упаковка продаётся не целиком?
В момент отпуска только части упаковки, происходит «частичное» выбытие вторичной упаковки. Она должна сохраняться до момента отпуска последней доли упаковки. Для этого необходимо ввести «долю» упаковки на кассовом ПО.
В случае обнаружения попытки осуществить вывод «излишка» система мониторинга зафиксирует нарушение!
Что делать, если покупатель отказался от покупки?
Бывает, так что покупка не состоялась (отказ по инициативе покупателя, отсутствие необходимой суммы денежных средств), а маркированный лекарственный препарат «пробит» на кассе в аптеке.
В этом случае чек не закрывается и должен быть аннулирован посредством программного обеспечения.
Операция пробития чека не состоялась — информация не передалась ОФД, поэтому сведения о выбытии товара в системе мониторинга не зафиксировались.

Заключение
Введение обязательной маркировки лекарственных средств было необходимым решением для снижения доли контрафактных и поддельных лекарственных средств в обороте. Перед проектом «Маркировка» стоят масштабные цели, но их достижение обеспечит результаты, в которых заинтересованы все участники жизненного цикла препарата.
Внедрение системы мониторинга и перестройка рабочего процесса изначально могут показаться сложными и пугающими. Но стоит запастись терпением, выполнять необходимые рекомендации, и в скором времени каждый сотрудник фармацевтической отрасли сможет оценить важность этого проекта.
Выводы
- Фармацевтическая отрасль столкнулась с маркировкой лекарств в 2015 году.
- Система МДЛП отслеживает движение лекарств от производителя до покупателя.
- Маркировка лекарств обеспечивает защиту от подделок и контроль качества.
- Система маркировки включает уникальный двухмерный Data Matrix код, соответствующий международным стандартам.
- Маркировка охватывает всё больше товаров аптечного ассортимента, включая лекарственные препараты, БАДы, детское питание и антисептики.
- Обязательная маркировка лекарств в России началась с 1 июля 2020 года.
- Система маркировки позволяет отслеживать путь лекарств от производителя до покупателя и проверять их подлинность.
- Участники системы маркировки включают производителей, оптовых компаний, розничных аптек и медицинских организаций.
Источники
- 1. Обязательная маркировка лекарственных средств — особенности;
- 2. Методические рекомендации по работе с маркированными лекарственными препаратами (утв. Росздравнадзором).
Проверь знания по статье

Другие статьи по теме «Работа в аптеке»
Смотреть все
Комментарии
Количество комментариев 7

Наталья Б.
Эксперт комьюнити ООО "Бережная аптека Апрель"
Сколько изменений произошло в фармотрасли за последние годы!Процесс маркировки-один из важных этапов работы,начиная от приемочного контроля,заканчивая конечным потребителем.Сейчас это не так страшно.как было в начале ,ждем продолжение в формате маркировки перчаток,шприцев,презервативов...
-

Юлия Б.
Эксперт комьюнити АС "Здесь Аптека"
Точно, согласна с вами, коллега.. а еще БАД, также с сентября поэкземплярный учет. С ними тоже сейчас проблемы бывают - то код стертый, то еще что-то. Будем ко всему адаптироваться потихоньку!
-

Светлана Ц. ООО Элифант
Как сложно всё....в русском словаре добавляются новые слова..."человекочитаемая" часть кода))) Спасибо, было интересно.

Юлия Б.
Эксперт комьюнити АС "Здесь Аптека"
Маркировка - достаточно объемная тема, это наши реалии, то, с чем мы столкнулись, как специалисты в 2019-2020 гг, когда маркировка по ЛП вступила в силу. Сейчас 2025 г - в этом году продолжается работа с маркировкой, все больше и больше ТАА уже маркируются, с сентября 2025 - поэкземплярный учет уже некоторых ТАА

Галина К. Фармленд
Спасибо за информацию!

Людмила Ж. Эркафарм
Спасибо !

Ольга С. Мелздрав Нижний Новгород
спасибо
Сайт носит обучающий (информационный) характер и предназначен исключительно для обучения (информирования) фармацевтов и провизоров









Авторизуйтесь, чтобы оставить комментарий.